Особенности состава продуктов гидратации композиционных портландцементов с карбонатсодержащими добавками
РЕФЕРАТ. В статье приведены результаты изучения составов продуктов гидратации портландцементов, содержащих минеральные добавки, с применением дифференциально-термического, термогравиметрического и рентгенографического методов анализа. Высказано предположение о возможности присутствия карбонат-ионов в продуктах гидратации композиционных портландцементов с карбонатными добавками.
Ключевые слова: композиционный портландцемент, карбонаты, гидратация.
Keywords: composite Portland cement, carbonates, hydration.
Введение
Для решения вопросов, связанных с широким использованием композиционных портландцементов, содержащих карбонатные добавки, для изготовления бетонов на их основе, твердеющих в различных условиях, необходимо выяснить химический механизм взаимодействия карбонатов с другими продуктами гидратации цементов.
Цель данной работы — попытаться уточнить состав продуктов гидратации цементов с карбонатными добавками.
Долгое время добавки карбонатов в цементы и бетоны относили к группе микронаполнителей, считая их химически инертными веществами, а основным продуктом, образующимся при действии углекислого газа на цементный камень, считался карбонат кальция CaCO3. Авторами работы [1] установлено, что при гидратации в нормальных условиях смеси портландцемента с тонкоизмельченным известняком в качестве одного из продуктов гидратации образуется гидрокарбоалюминат кальция 3CaO · Al2O3 · CaCO3 · 11H2O. При взаимодействии с доломитом может образоваться аналогичное соединение 3CaO · Al2O3 · MgCO3 · 11H2O. Авторы отмечали, что при температуре выше 100 °С эти соединения начинают разлагаться.
Основным продуктом взаимодействия CaCO3 c водой в присутствии СО2 является растворимый гидрокарбонат кальция Ca(НCO3)2 [2], в растворе которого находятся ионы CaНCO3+ и НCO3–, в связи с чем, по нашему мнению, не исключено, что в момент образования новые гидратные фазы имеют состав 3CaO · Al2O3 · Ca(НCO3)2 · nH2O.
Гидрокарбонат кальция — нестойкое вещество, которое при продолжительном нахождении его раствора на воздухе или при повышении температуры до 95—100 °С разлагается с выделением воды и углекислого газа и образованием средней соли CaCO3. Если принять, что первоначальный состав образовавшейся двойной соли — 3CaO · Al2O3 · Ca(НCO3)2 · nH2O, то только после подобных изменений, сопровождающихся выделением молекул Н2О и СО2, ее окончательный состав может соответствовать формуле, предложенной в работе [1]. Видимо, такое преобразование было обнаружено авторами этой работы, отмечавшими, что гидрокарбоалюминаты кальция начинают разлагаться при температуре выше 100 °С. Подобное разложение этих соединений может отрицательно влиять на свойства бетонов, твердеющих в условиях пропаривания.
С тех пор когда в составе продуктов гидратации портландцементов с карбонатными добавками были обнаружены новообразования в виде гидрокарбоалюмината кальция, для изготовления таких цементов рекомендуется в основном применять клинкеры с повышенным до 10—13 % содержанием трехкальциевого алюмината [3]. По этой же причине чаще всего влияние карбонатсодержащих добавок на состав продуктов гидратации цементов связывают с составом гидратных фаз, образующихся при взаимодействии продуктов гидратации трехкальциевого алюмината с указанными добавками, априори исключая возможность участия этих добавок в формировании продуктов гидратации силикатных фаз. При гидратации трехкальциевого алюмината в присутствии карбонатных добавок, бесспорно, может образовываться гидрокарбоалюминат кальция; возможно также образование твердых растворов между гидрокарбоалюминатом кальция и гидроксоалюминатом кальция состава 3CaO · Al2O3 · Ca(ОН)2 · 11H2O [4]. Не исключается также возможность замещения части сульфатных ионов в составе эттрингита на карбонатные ионы. Однако необходимо учитывать, что в портландцементных клинкерах, производимых цементными заводами России, расчетное содержание трехкальциевого алюмината составляет 7,0—8,0 %, а фактическое содержание этого минерала в большинстве клинкеров — 5,0—6,0 % [5].
Кроме того, по данным многих авторов, в продуктах гидратации цементно-кремнеземистых материалов часть Al2O3 входит в фазу C—S—H [6]. В связи с этим можно считать, что при гидратации С3А в присутствии карбонатных добавок может образоваться лишь незначительное количество гидрокарбоалюминатной фазы, которая не будет определяющим образом влиять на свойства цементного камня.
Продукты гидратации кальциево-силикатных фаз, взаимодействуя с угольной кислотой и ее солями, образуют новые соединения — гидрокарбосиликаты кальция, состав которых к настоящему времени недостаточно изучен. Авторами работы [7] показано, что в ходе карбонизации цементного камня самое большое количество СО2 поглощается продуктами гидратации С3S, а в составе образующихся новых фаз отмечается наличие гидрокарбосиликатов кальция.
Отметим, что состав образующихся в ходе гидратации цемента гидросиликатных фаз трудно идентифицировать при помощи современных инструментальных методов, так как эти фазы представляют собой рентгеноаморфные неорганические полимеры.
По нашему мнению, карбонаты могут взаимодействовать с продуктами гидратации силикатов, составляющими фазу С—S—H, в форме Ca(НCO3)2, диссоциирующего на ионы CaHCO3+ и HCO3–. С течением длительного времени или при повышении температуры до 80—100 °С возможны разложение гидрокарбонатных групп с выделением СО2 и Н2О и образование гидрокарбосиликата кальция. Представителем этой группы соединений является встречающаяся в природе двойная соль — минерал скаутит Ca5[Si6O17] · Ca(OH)2 · CaCO3 · nH2O, который часто обнаруживали в системе CaO—SiO2—H2O, загрязненной СО2. В литературе гидраты кальциево-силикатных фаз, представляющие собой двойные соли, часто называют гидросиликатами с добавочными ионами [8].
Об активном взаимодействии гидросиликатов кальция с углекислым газом свидетельствуют результаты ранее выполненных исследований [9]: в ходе принудительной карбонизации гидратных фаз, полученных при автоклавной обработке известково-кварцевых смесей, за 60 ч связывается количество СО2, соответствующее 50 %-й степени карбонизации всего СаО, находящегося в продуктах гидратации. При наличии добавок гипса или хлорида кальция связывание СО2 протекает еще активнее и достигается степень карбонизации около 70 %. Наименьшее количество СО2 поглощают продукты взаимодействия известково-кварцевых смесей, если в их составе имеется добавка карбоната кальция. На дериватограммах продуктов карбонизации всех смесей основным был глубокий эндотермический эффект со значительной потерей массы при температуре 100—120 °С. Эндотермический эффект при температуре 860—880 °С, соответствующий разложению СаСО3, сопровождался потерей массы, которая в 2—3 раза меньше массы связанного СО2.
Если фаза C—S—H содержит в своем составе алюминий, то при взаимодействии с гидрокарбонатом кальция может образоваться алюминийсодержащий гидрокарбосиликат кальция.
Среди возможных новых гидратных фаз, способных образоваться в ходе гидратации композиционных портландцементов с карбонатными добавками, значительную долю могут составлять гидроксокарбонат кальция — Са(ОН)2 · СаСО3 · nН2О, минерал дефернит [6] и его аналог — Са(ОН)2 · MgСО3 · nН2О. По всей вероятности, эти фазы образуются в первую очередь, так как жидкая фаза цементного теста за счет гидролиза C3S содержит значительное количество Са(ОН)2. За счет образования этих соединений в цементном камне, полученном из композиционного портландцемента с карбонатными добавками, содержание свободного Са(ОН)2 значительно меньше, чем в цементном камне из портландцемента с добавкой такого же количества гранулированного доменного шлака (ГДШ). По нашему мнению, эти фазы, по аналогии с другими новообразованиями, имеют первоначальный состав Са(ОН)2 · Са(НСО3)2 · nН2О и Са(ОН)2 · Mg(НСО3)2 · nН2О и претерпевают со временем или с повышением температуры сходные изменения — гидрокарбонатная группа в их составе превращается в карбонатную.
При одновременном наличии карбонатных добавок и достаточного количества гипса могут образоваться продукты гидратации цементных фаз, в составе которых одновременно присутствуют сульфатные и карбонатные анионы. Возможность образования таких сложных гидратов на основе продуктов гидратации C3A в виде твердых растворов AFt-фаз предполагается в работе [4]. По нашему мнению, они могут также образоваться в результате реакций с участием гидрокарбонатов и последующего разложения гидрокарбонатных групп при повышении температуры с выделением воды и углекислого газа.
Поскольку в составе всех композиционных портландцементов с карбонатными добавками имеется добавка гипса, при гидратации таких цементов нельзя исключать возможность образования некоторого количества таумасита СаН2SiО4 · СаSО4 · CаСО3 · 14Н2О.
Все описанные новообразования могут способствовать созданию оптимального соотношения гелеобразных и хорошо закристаллизованных фаз, что необходимо для формирования прочной структуры. Кроме того, при пониженном содержании гипса на самой ранней стадии гидратации будет образовываться значительно меньшее количество эттрингита.
Экспериментальная часть и обсуждение результатов
Состав продуктов гидратации цемента контрольного состава, содержащего 20 % ГДШ, и композиционного портландцемента, содержащего комплексную добавку, состоящую из 10 % ГДШ и 10 % доломита (добавка гипса в том и другом цементе составляет 5 %), твердевших в нормальных условиях, изучен при помощи дифференциально-термического, термогравиметрического и рентгенографического анализов.
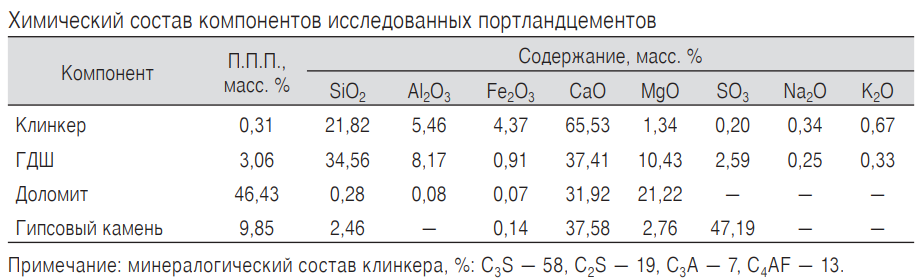
Для изготовления цементов использовались портландцементный клинкер цементного завода ОАО «Искитимцемент» (коэффициент насыщения — 0,9; силикатный модуль — 2,2; глиноземный модуль — 1,25), ГДШ (г. Новокузнецк), доломит Таензинского месторождения, гипсовый камень Ергачинского месторождения. Химический состав компонентов приведен в таблице.
Портландцемент изготавливали путем совместного помола компонентов в шаровой мельнице. Образцы-кубы размером 2 × 2 × 2 см формовались из теста нормальной густоты и твердели в течение 28 сут в нормальных условиях, затем их выдерживали 14 сут на воздухе, после чего растирали до полного прохождения через сито с размером ячеек 0,08 мм.
Дифференциально-термический и термогравиметрический анализы выполнены на дериватографе системы Paulik—Paulik—Erdey в неокислительной среде. Параметры съемки: верхний температурный предел — 1000 °С, скорость нагрева — 10 °С/мин. Интенсивность термических эффектов, сопровождающих реакции, и значения потерь массы использовались в качестве основы для количественного определения фаз.
Дериватограммы продуктов гидратации цементов приведены на рис. 1 и 2.
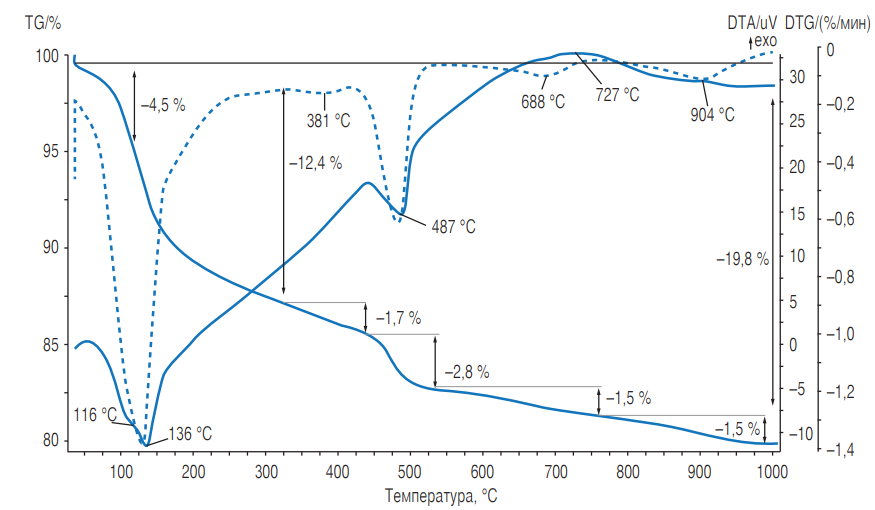
Рис. 1. Дериватограмма продуктов гидратации цемента состава: клинкер + 20 % ГДШ + гипс в возрасте 28 сут
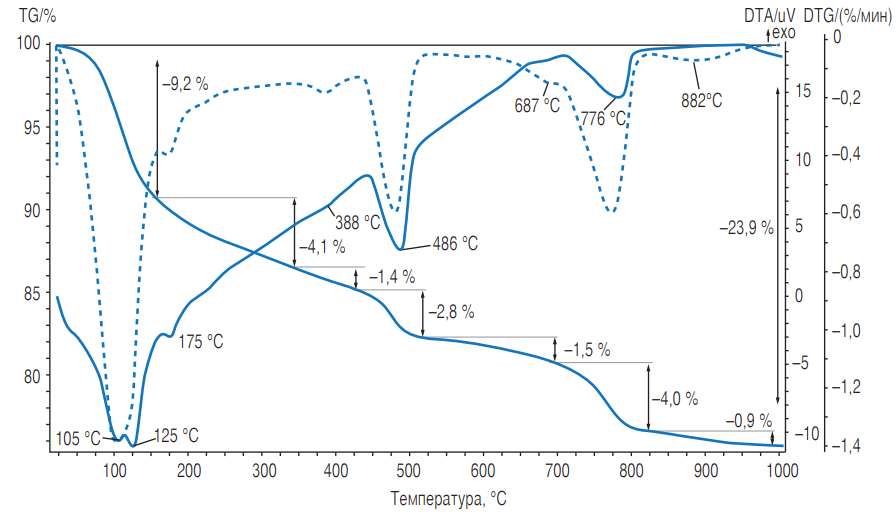
Рис. 2. Дериватограмма продуктов гидратации цемента состава: клинкер + 10 % ГДШ + 10 % доломита + гипс в возрасте 28 сут
На кривой ДТА продуктов гидратации цемента контрольного состава имеются три эндотермических эффекта, два слившихся эндотермических эффекта при температуре 116 и 136 °С и эндотермический эффект при 487 °С. Эндотермический эффект при 116 °С может соответствовать удалению химически связанной воды из состава гидросиликатной фазы, эндотермический эффект при 136 °С — удалению части воды из эттрингита [10]. Эндотермический эффект при 487 °С соответствует удалению воды из свободного гидроксида кальция. На кривой ДТА продуктов гидратации композиционного портландцемента с добавкой доломита четко выделились в области низких температур два самостоятельных эндотермических эффекта, при 105 и 125 °С. Считаем, что эндоэффект при 105 °С соответствует разложению гидрокарбоната кальция и гидрокарбонатных групп, входящих в состав других гидратных фаз. Эндотермический эффект при 125 °С может соответствовать удалению воды из гидросиликатов различного состава. В продуктах гидратации этого цемента, вероятно, уменьшилось количество эттрингита, так как при температуре 175 °С возник эндотермический эффект, характерный для гидрокарбоалюмината кальция 3СаО · Al2O3 · CaCO3 · 12H2O [10]. Возможно, что этот эффект отражает также наличие гидрокарбоалюминатных групп в составе фазы С—S—H.
Поскольку композиционный портландцемент содержит добавку доломита, на кривой ДТА присутствуют его эндотермические эффекты (при температуре выше 500 °С). Приведем пример расчета ориентировочного количества доломита, взаимодействующего с продуктами гидратации портландцемента: на дериватограмме цементного камня, изготовленного из портландцемента, содержащего 20 % ГДШ, потеря массы при температуре выше 500 °С составляет 3,0 %. Шлак при такой температуре не теряет массу. При замене половины шлака доломитом (т. е. при содержании доломита 10 %) потеря массы должна увеличиться на 4,6 % (П.П.П. доломита — 46,43 %, см. таблицу), приблизительно до 7,6 %, а фактически она равна 6,4 % (см. рис. 2). Уменьшение потери массы по сравнению с расчетным значением составляет 1,2 %. Из этого можно сделать вывод, что при указанной температуре происходит декарбонизация 74 % введенного доломита, а остальная часть израсходована в реакциях взаимодействия с продуктами гидратации цемента.
На рентгенограммах исследуемых проб гидратированных цементов основные дифракционные максимумы принадлежат остаткам негидратированного алита (3,03; 2,77; 2,60)·10–10 м. Из образовавшихся продуктов гидратации идентифицируется только гидроксид кальция (4,90; 2,63; 1,93)·10–10 м. Остальные продукты гидратации являются слабо закристаллизованными фазами. На рентгенограмме гидратированного композиционного портландцемента с карбонатной добавкой дополнительно присутствуют слабый дифракционный максимум гидрокарбоалюмината кальция (7,60)·10–10 м и максимумы доломита (2,88; 2,19; 1,79)·10–10 м.
Заключение
Результаты дифференциально-термического анализа указывают на то, что состав продуктов гидратации портландцемента, содержащего ГДШ, изменяется при замене части ГДШ на карбонатную добавку. Не исключено, что в состав фаз, образующихся при гидратации, входят карбонат-ионы. Для уточнения состава образующихся фаз необходимы дополнительные исследования.
Выполненные расчеты по результатам термогравиметрического анализа показывают, что при наличии в композиционном портландцементе 10 % доломита после 28 сут гидратации цемента в нормальных условиях сохраняется непрореагировавшим около 7,4 % доломита.
ЛИТЕРАТУРА
1. Будников П.П., Колбасов В.М., Пантелеев А.С. Взаимодействие 3СаО·Al2O3 и 4СаО·Al2O3·Fe2O3 c карбонатами кальция и магния // ДАН СССР. 1959. Т. 129, № 5. С. 1104—1106.
2. Глинка Н.Л.. Общая химия. Л.: Химия, 1981. 440 с.
3. Пантелеев А.С., Колбасов В.М.. Цементы с минеральными добавками-микронаполнителями // Новое в химии и технологии цемента. М.: Стройиздат, 1962. С. 155—164.
4. Сивков С.П. Термодинамический анализ фазообразования при твердении карбонатсодержащих цементов // Цемент и его применение. 2008. № 4. С. 112—115.
5. Козлова В.К., Григорьев В.Г., Малова Е.Ю., Божок Е.В., Мануйлов Е.В. Сравнительные результаты определения фазового состава и микроструктуры клинкеров современными методами физико-химического анализа // Цемент и его применение. 2013. № 3. С. 34—38.
6. Тейлор Х.Ф.У. Химия цемента. М.: Мир, 1996. 430 с.
7. Самченко С.В., Макаров Е.М. Карбонизация гидратных составляющих портландцемента, алюминатного и сульфоалюминатного цементов // Техника и технология силикатов. 2013. № 3. С. 27.
8. Тейлор Х.Ф.У. Гидросиликаты кальция // Пятый Междунар. конгр. по химии цемента. М., 1973. С. 123.
9. Козлова В.К., Карпова Ю.В., Ильевский Ю.А. Продукты гидратации кальциево-силикатных фаз цемента и смешанных вяжущих веществ. Барнаул: Изд-во АлтГТУ, 2005. 163 с.
10. Горшков В.С., Тимашев В.В., Савельев В.Г. Физико-химические методы анализа вяжущих веществ М.: Высшая школа, 1981. 333 с.
| Автор: В.К. Козлова, А.М. Маноха, В.П. Скакун, Е.Ю. Малова, Е.В. Божок |
| Рубрика: Наука и производство |
| Ключевые слова: композиционный портландцемент, карбонаты, гидратация |




